A válvula mecanicamente expansível Lotus Edge foi descontinuada em todo o mundo de acordo com informação recente de seu produtor, a Boston Scientific.
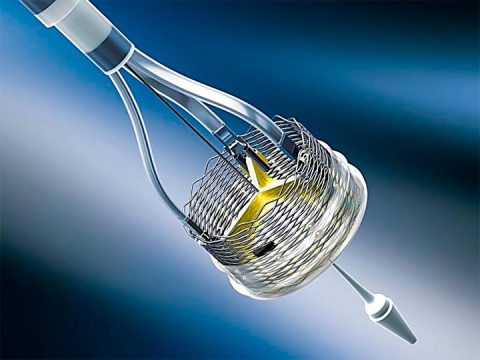
Este é um “recall” voluntário de todo o inventário da válvula Lotus, além da imediata suspensão do programa.
A FDA (US Food and Drug Administration) aprovou a Lotus Edge no ano 2019 para pacientes com estenose aórtica severa sintomática e alto risco cirúrgico. A válvula já tinha o CE Mark europeu desde 2016.
O design desta válvula tão especial sempre foi muito desafiante, sobretudo o sistema de liberação, o que levou a Boston a remediar o problema suspendendo o programa. Agora toda a atenção da Boston vai se centrar na Acurate neo.
Os benefícios da válvula, especialmente em termos de regurgitação paravalvar, eram inegáveis, mas sua liberação e recaptura eram muito complexas.
O dispositivo Lotus já tinha sofrido retiradas do mercado em 2016 por falhas no sistema de liberação e em 2017 por falhas no sistema de oclusão.
Leia também: Cirurgia bariátrica por cateterismo?
Esta última e definitiva retirada também se deveu a problemas com o sistema de liberação. Dado o tempo e os custos necessários para desenvolver soluções e introduzi-las no mercado, a companhia decidiu retirar o produto.
A Boston esclarece no anúncio que não há nenhum problema de segurança para os pacientes que têm uma Lotus implantada.
A companhia vai continuar com a pesquisa da Acurate Neo, embora os estudos SCOPE e SCOPE 2, que testaram a primeira geração da válvula da Boston vs. a Sapien 3 e a CoreValve Evolut, respectivamente não tenham alcançado a não inferioridade.
Leia também: Veja novamente Novas Fronteiras na Sala de Hemodinâmica.
Agora a resposta está na Acurate Neo 2, com 2 melhoras para diminuir a regurgitação paravalvar.
Título original: Boston Scientific announces Lotus Edge aortic valve system voluntary recall and product discontinuation.
Referência: Boston Scientific. Published on: November 2020.
Subscreva-se a nossa newsletter semanal
Receba resumos com os últimos artigos científicos





