El cierre percutáneo de orejuela izquierda (LAAO) con dispositivo Watchman cuenta con aprobación de la FDA desde marzo de 2015, habiendo demostrado, en los estudios PROTECT-AF y PREVAIL, una disminución en el riesgo de ACV relacionado a fibrilación auricular, al excluir la orejuela izquierda de la circulación sistémica.
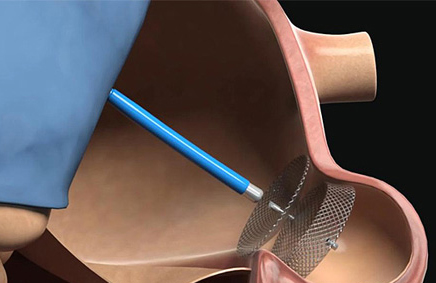
En ambos trabajos se usaron protocolos estandarizados en el post procedimiento, que incluía un seguimiento específico a los 45 días y 6 meses, imágenes y un esquema antitrombótico determinado. Por lo cual, la FDA elaboró determinadas sugerencias que consistían en: tratamiento antitrombótico al egreso hospitalario con warfarina y aspirina (80-325mg) por 45 días post implante, ecocardiograma transesofágico en el primer control (45 días) y en caso de presentar leak peridispositivo >5mm continuar con mismo esquema antitrombótico, caso contrario, se continuaba antiagregación con terapia antiplaquetaria dual (DAPT) con clopidogrel por 6 meses.
Como se suelen presentar, los pacientes de la vida real presentan diferencias importantes de aquellos incluidos en los trials, debido a edad y comorbilidades (más eventos de sangrado). Por este motivo, posterior a la aprobación del dispositivo se realizó el registro nacional americano de datos cardiovasculares de LAAO (NCDR). En el mismo, se observaron variaciones respecto al tratamiento y seguimiento por protocolo sugerido por la FDA.
El objetivo de este estudio fue evaluar la desviación y los distintos esquemas usados en los pacientes de la vida real, a través del registro NCDR, que incluyó pacientes de 2016 a 2018 con el primer dispositivo de Watchman.
El punto final primario (PFP) consistió en cualquier efecto adverso (eventos neurológicos, pulmonares o cardiovasculares o de sangrado), efecto adverso mayor (muerte, paro cardiorespiratorio, IAM, derrame pericárdico significativo, embolia sistémica, stroke o sangrado mayor), stroke o AIT y/o readmisión a los 45 días. El punto final secundario incluyó los mismos eventos que el primario, pero en un seguimiento a 6 meses.
Se analizaron datos de 31994 pacientes, edad promedio de 76 años, CHADS-VASC promedio de 4.6 y HAS-BLED=3. Solo 12.2% siguieron todos los lineamientos aprobados por la FDA (tratamiento y seguimiento), principalmente a expensas del tratamiento antitrombótico distinto al sugerido de warfarina y aspirina (61.5%). Las estrategias post implante evaluadas fueron warfarina y aspirina (36.9%), anticoagulante directo (DOAC) y aspirina (20.8%), warfarina sola (13.5%), DOAC solo (12.3%) y DAPT (5%).
El índice de aparición de cualquier efecto adverso no ajustado fue mayor entre los tratados con warfarina y aspirina (5.7%) seguido por DAPT (5.6%), principalmente a expensas de eventos de sangrado, sin presentar diferencias en stroke o AIT. En el análisis de regresión, el riesgo ajustado de cualquier evento adverso a los 45 días fue significativamente menor en el grupo warfarina sola (HR: 0.692; IC 95% 0.569-0.841) y DOAC solo (HR: 0.731; IC 95% 0.574-0.930) en relación a warfarina más aspirina.
El riesgo de cualquier evento adverso mayor fue significativamente menor con warfarina (HR: 0.658; IC 95% 0.536-0.808) y DOAC (HR: 0.767; IC 95% 0.597-0.985), sin presentar mayor riesgo de stroke, AIT o leak peridispositivo >5mm.
En el seguimiento a 6 meses se observó menor cantidad de eventos en el grupo warfarina, sin presentar riesgo de stroke o AIT.
Conclusiones
En este registro, que contó con 70% de pacientes con algún antecedente de sangrado, con un HAS-BLED promedio de 3, se observó que se respetó el tratamiento sugerido por la FDA de warfarina y aspirina solo en un 37% de los casos. A su vez, la estrategia antitrombótica de warfarina sola o DOAC solo mostró menor cantidad de eventos, con una incidencia de stroke o AIT similar comparado con warfarina más aspirina.
Aclarar que este registro no cuenta con los datos del dispositivo Watchman FLX, si no de la primera generación, a diferencia del estudio PINNACLE FLX (elección de DOAC más aspirina como antitrombóticos).

Dr. Omar Tupayachi.
Miembro del Consejo Editorial de SOLACI.org.
Título Original: Antithrombotic Therapy After Left Atrial Appendage Occlusion in Patients With Atrial Fibrillation
Fuente: Freeman JV, Higgins AY, Wang Y, Du C, Friedman DJ, Daimee UA, Minges KE, Pereira L, Goldsweig AM, Price MJ, Reddy VY, Gibson D, Doshi SK, Varosy PD, Masoudi FA, Curtis JP. Antithrombotic Therapy After Left Atrial Appendage Occlusion in Patients With Atrial Fibrillation. J Am Coll Cardiol. 2022 May 10;79(18):1785-1798. doi: 10.1016/j.jacc.2022.02.047.
Suscríbase a nuestro newsletter semanal
Reciba resúmenes con los últimos artículos científicos





