La válvula balón expandible logró su aprobación en Europa para tratar el espectro completo de riesgo de pacientes con estenosis aórtica severa sintomática.
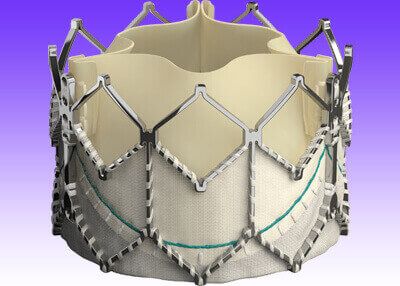
Europa expandió la indicación del sistema Sapien 3 para su uso en pacientes de bajo riesgo según informó Edward Lifesciences en estos días.
La Sapien 3, que incluye la siguiente generación Sapien 3 ultra, es la primera válvula transcatéter en recibir el CE Mark en pacientes de bajo riesgo quirúrgico. El dispositivo ahora tiene la aprobación para todos los pacientes, incluyendo los de riesgo intermedio, alto y aquellos descartados de cirugía.
Para expandir la indicación de la Sapien 3 se basaron en los resultados del estudio PARTNER 3, que fue presentado durante las sesiones científicas del congreso de la American College of Cardiology en marzo de este año y publicado simultáneamente en NEJM.
En este trabajo se incluyeron unos 1000 pacientes de bajo riesgo, probando que el TAVI se asoció a un menor y significativo riesgo del end point combinado de muerte, stroke y re-hospitalizaciones comparado con la cirugía de reemplazo valvular.
En este agosto la FDA aprobó, basándose en el mismo trabajo, a la Sapien 3 y la Sapien 3 ultra, pero también incluyó a la válvula auto-expandible CoreValve, Evolut R y Evolut Pro (todas de Medtronic) basándose en los resultados del Evolut Low-Risk presentado también en el ACC y publicado también en NEJM.
Por ahora la válvula de Medtronic tiene que esperar en Europa su aprobación, pero esto solo parece una cuestión administrativa.
Una vez más el TAVI muestra, en varios sentidos, recorrer el camino inverso a la mayoría de los dispositivos que utilizamos. De comenzar con los pacientes más difíciles para luego llegar a los más fáciles, de conseguir primero la aprobación de la FDA y después el CE mark.
Título original: Edwards Sapien 3 TAVI receives expanded approval in Europe.
Referencia: Edwards Lifesciences. Published and accessed on: November 6, 2019.
Suscríbase a nuestro newsletter semanal
Reciba resúmenes con los últimos artículos científicos





