La válvula mecánicamente expandible Lotus Edge fue discontinuada en todo el mundo según informó recientemente su productor Boston Scientific.
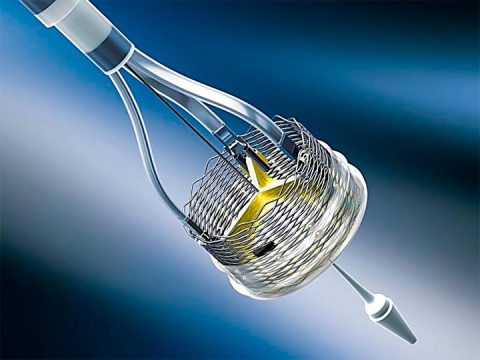
Este es un “recall” voluntario de todo el inventario de la válvula Lotus, además de la inmediata suspensión del programa.
La FDA (US Food and Drug Administration) aprobó la Lotus Edge en el año 2019 para pacientes con estenosis aórtica severa sintomática y alto riesgo quirúrgico. La válvula ya tenía el CE Mark de Europa desde 2016.
El diseño de esta válvula tan especial siempre fue muy desafiante, sobre todo el sistema de liberación, lo que llevó a Boston a cortar por lo sano y suspender el programa. Ahora toda la atención de Boston se va a centrar en la Acurate neo.
Los beneficios de la válvula, especialmente en términos de leaks paravalvulares, eran innegables pero su liberación y recaptura era desafiante.
El dispositivo Lotus ya había sufrido retiros del mercado en 2016 por fallas en el sistema de liberación y en 2017 por fallas en el sistema de cierre.
Lea también: ¿Cirugía bariátrica por cateterismo?
Este último y definitivo retiro también se debió a problemas con el sistema de liberación. Dado el tiempo y los costos necesarios para desarrollar e introducirlo en el mercado, Boston decidió directamente retirar el producto.
Boston aclara en el documento que no hay ningún problema de seguridad para los pacientes que ya tienen implantada una Lotus.
La compañía va a continuar con la investigación de la Acurate Neo, aunque los estudios SCOPE y SCOPE 2 que testearon la primera generación de la válvula de Boston vs Sapien 3 y CoreValve Evolut, respectivamente no alcanzaron la no inferioridad.
Lea también: Vuelva a ver Nuevas Fronteras en la Sala de Hemodinamia.
Ahora la apuesta está en la Acurate Neo 2 con mejoras para disminuir los leaks paravalvulares.
Título original: Boston Scientific announces Lotus Edge aortic valve system voluntary recall and product discontinuation.
Referencia: Boston Scientific. Published on: November 2020.
Suscríbase a nuestro newsletter semanal
Reciba resúmenes con los últimos artículos científicos





